‘Theoretische achtergronden Ketelwater’
2.1 Ontharding
Onbehandeld water bevat meestal een bepaalde hoeveelheid hardheid. Hardheid is gedefinieerd als de som van tijdelijke hardheid en blijvende hardheid.
De tijdelijke hardheid zijn alle calcium- en magnesiumbicarbonaten.
De blijvende hardheid zijn alle overige calcium- en magnesiumzouten.
De tijdelijke hardheid zal bij verhoging van de watertemperatuur kalk vormen, dat als harde, isolerende afzetting neerslaat op vooral de heetste delen van de stoomketel.
Om te voorkomen dat kalk in de ketel ontstaat kan het suppletiewater onthard worden.
Ontharding geschiedt door alle calcium- en magnesiumionen te vervangen door natrium, middels een klassieke onthardingsinstallatie.
2.2 Decarbonatatie
Decarbonatatie heeft net als ontharding ionenwisseling als principe.
Wordt bij ontharding Calcium en Magnesium uitgewisseld tegen Natrium; bij decarbo-natatie worden positieve ionen tegen waterstofionen (H+) of alle bicarbonaat- (HCO3-) en carbonaationen (CO32-) tegen chloride-ionen uitgewisseld. Resultaat is dat calcium-carbonaat (kalk) niet meer kan neerslaan in de ketel omdat het bicarbonaat verwijderd is.
Indien een sterk zure harsmassa gekozen wordt zullen alle positieve ionen worden uitge-wisseld tegen H+, waarbij mineraalzuur ontstaat.
Is de harsmassa zwakzuur, dan zullen alleen de positieve ionen in verbinding met het zwak-zure bicarbonaat (HCO3-) worden uitgewisseld waardoor de blijvende hardheid blijft bestaan.
Achter een (zure) decarbonatatie-installatie dient een uitdrijftoren te worden geplaatst om het ontstane CO2 te laten ontwijken. Hiertoe is een optimale menging met lucht noodzake-lijk. Regeneratie vindt plaats met zoutzuur (HCl).
2.3 Demineralisatie
Het principe van ontzouting middels demineralisatie is ook gebaseerd op het uitwisselen van ionen.
Alle positieve ionen én negatieve ionen worden hierbij vervangen door respectievelijk H+ (waterstofion) en OH- (hydroxylion) welke tezamen H2O vormen.
Er zijn dan ook twee types hars nodig.
Het kationhars is beladen met H+-ionen en het anionhars met OH–ionen.
Regeneratie geschiedt met natronloog (NaOH) voor de anionzuil en met zoutzuur (HCl) voor de kationzuil.
2.4 Reverse Osmosis (R.O.)
Reverse Osmosis (omgekeerde osmose) is gebaseerd op de osmotische druk van water.
Indien twee zoutoplossingen van verschillende concentraties door een semi-permeabel membraan (alleen passeerbaar voor water moleculen) gescheiden worden, zal water van de oplossing met de laagste zoutconcentratie door het membraan naar die met de hoogste concentratie gaan. Op deze manier zal de osmotische druk in de hoogste concentratie verlagen en dus het verschil tussen hoog en laag verkleinen. Wordt nu op het water met de hoogste zoutconcentratie een druk uitgeoefend welke groter is dan de osmotische druk, dan zal de waterstroom door het membraan omkeren (omgekeerde (reverse) osmose). Bij toepassing van dit principe verkrijgt men zeer zoutarm water.
Indien het oorspronkelijke water een hoge hardheid heeft dient dit vooronthard of van een antiscalant voorzien te worden om kalkafzetting op het membraan te voorkomen.
2.5 Thermische ontgassing
Het ontgassen van het ketelvoedingswater is noodzakelijk om schadelijke gassen uit het voedingswater te verwijderen. De schadelijke gassen zijn in dit geval zuurstof en vrij koolzuurgas.
Beide gassen moeten uit het voedingswater worden verwijderd in verband met corrosie, die zij in het verdere deel van de ketelinstallatie kunnen veroorzaken.
Met het ontgassen wordt daarom beoogd in het voedingwater het zuurstofgehalte te verlagen tot minder dan 0,1 mg/l en het koolzuurgehalte tot minder dan 5 mg/l. Dit zijn de richtlijnen zoals die gelden voor voedingswater ten behoeve van stoomketelinstallaties tot circa 20 bar werkdruk.
Ontgassing van het ketelvoedingswater geschiedt door verwarming van het water onder druk of vacuüm. Men maakt hierbij gebruik van het principe dat de oplosbaarheid van gassen in water bij temperatuurverhoging afneemt. Dit fysische proces vindt plaats in een gesloten tank.
3.1 Bicarbonaat- en sodasplitsing
De bicarbonaat- en sodasplitsing is voor het ketelbedrijf van groot belang, omdat dit de bron is voor het koolstofdioxide (CO2) in de gecondenseerde stoom. Dit koolstofdioxide is in belangrijke mate verantwoordelijk voor de aantasting van condensaatleidingen en appara-tuur.
Bevat het voedingswater van een stoomketel geen hardheid, dan is het bicarbonaat gebonden aan natrium. Reeds in de ontgasser vindt ten gevolge van de hoge temperatuur deels een chemische omzetting plaats van het natriumbicarbonaat in koolstofdioxide en natriumcarbonaat (soda), volgen+s onderstaande reactievergelijking:
2NaHCO3 —> Na2CO3 + CO2 + H2O “bicarbonaat-splitsing”
Het gevormde koolstofdioxide wordt in de ontgasser uitgedreven, hetgeen gunstig is.
Ten gevolge van de gedeeltelijke ontleding van het natriumbicarbonaat in natrium-carbonaat, gaat vervolgens een mengsel van natriumbicarbonaat en natriumcarbonaat naar de ketel.
Onder invloed van de aldaar heersende druk en temperatuur, wordt het resterende deel natriumbicarbonaat omgezet in natriumcarbonaat (soda). Dit natriumcarbonaat wordt vervolgens omgezet tot natriumhydroxide en koolstofdioxide, volgens onderstaande reactievergelijking:
Na2CO3 + H2O —> 2NaOH + CO2 “soda-splitsing”
Het gevormde natriumhydroxide (loog) geeft alkaliteit aan het ketelwater en veroorzaakt het P-getal. Het koolstofdioxide gaat met de stoom mee en lost naderhand op in het condensaat onder de vorming van koolzuur conform de vergelijking:
CO2 + H2O <===> H2CO3 <===> HCO3- + H+
Hierdoor wordt de zuurgraad (pH) van het condensaat verlaagd en dit zure condensaat geeft aanleiding tot egale corrosie, waarbij de wanddikte van leidingen en apparatuur geleidelijk afneemt.
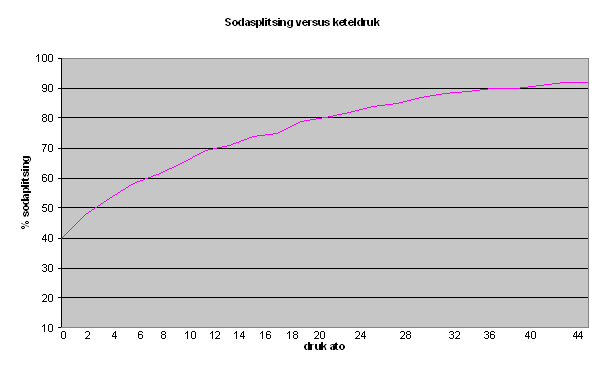
De “soda-splitsing” is een functie van de keteldruk en neemt toe naarmate de druk hoger is (zie afbeelding). De “soda-splitsing” is echter onafhankelijk van de verblijftijd van het water in de ketel.
3.2 Indikking van het ketelwater
Het voedingswater dat van de ketelvoedingswatertank of de ontgasser naar de ketel gaat, bevat een hoeveelheid zouten en andere componenten. In de ketel wordt stoom geproduceerd, hetgeen in principe vergelijkbaar is met een destillatie proces. De geproduceerde stoom bestaat uit zuiver water en de in het water aanwezige zouten blijven dus achter in de ketel. Zou men de voedingswatertoevoer naar de ketel stoppen en doorgaan met stoom produceren, dan wordt de concentratie van de opgeloste zouten steeds groter. Uiteindelijk zullen de oplosbaarheidgrenzen van de verschillende zouten overschreden worden en gaan deze over in vaste stoffen. Tenslotte zou men slechts een vaste massa overhouden. Ook indien men steeds voedingswater toevoert, zal op een gegeven moment de oplosbaarheidgrens van bepaalde componenten overschreden worden. Men heeft het water dan te ver laten indikken. Men dient dan ook, om de concentraties in het ketelwater binnen bepaalde grenzen te houden, regelmatig een bepaalde hoeveelheid ketelwater af te voeren door te spuien.
De hoeveelheid te spuien ketelwater, wordt bepaald door meetbare parameters, zoals die door bijvoorbeeld fabrikanten van stoomketels in richtlijnen zijn opgesteld. Het naar de ketel teruggevoerde condensaat, bevat normaliter praktisch geen zouten en bij een volledig gesloten systeem, waarbij geen verliezen optreden, zou het spuien derhalve niet nodig zijn. Zodra er echter verliezen zijn in de vorm van water of stoom, zal men vers water moeten suppleren. Het suppletiewater bevat, op bepaalde uitzonderingen na, een hoeveelheid zouten en staat dus in direct verband met de hoeveelheid te spuien ketelwater.
Ten gevolge van een ongecontroleerde hoge indikking en dus een toenemende zoutconcentratie in het ketelwater, kunnen diverse problemen ontstaan, die hoge kosten met zich meebrengen
3.3 Afzettingen
Ten gevolge van een te hoge indikking, kunnen de oplosbaarheidgrenzen van bepaalde zouten overschreden worden, met afzettingen in de ketel tot gevolg.
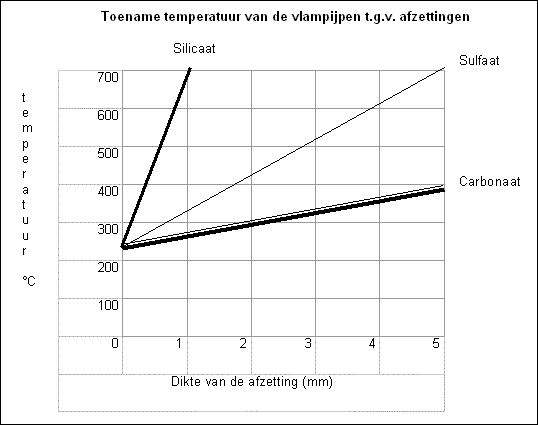
Daar afzettingen een veel lagere warmtegeleidingcoëfficiënt hebben dan het ketelmateriaal zelf (zie tabel), heeft dit tot gevolg dat op plaatsen waar zich afzettingen bevinden, de warmte minder goed kan worden uitgevoerd. Dit kan oververhitting en materiaalspanning tot gevolg hebben en uiteindelijk leiden tot schade aan de ketel. Tevens vermindert het rendement van de ketel sterk, hetgeen een verhoging van de energiekosten tot gevolg heeft.
3.3.1 Calciumcarbonaat
Calciumcarbonaat in ketelwatersystemen ontstaat doordat calciumbicarbonaat ten gevolge van temperatuur en druk wordt omgezet in calciumcarbonaat, koolstofdioxide en water conform onderstaande reactievergelijking.
Ca(HCO3)2 —> CaCO3 + CO2 + H2O
Daar de oplosbaarheidgrens van het calciumcarbonaat zeer laag is, kan zelfs bij toepassing van zacht water bij lage indikking reeds afzetting ontstaan. Het gevormde koolstofdioxide gaat met de stoom mee en kan problemen in het condensaatnet veroorzaken.
3.3.2 Magnesiumhydroxide
Wat voor calciumbicarbonaat geldt, is ook van toepassing op magnesiumbicarbonaat. Het calciumbicarbonaat zet zich als een harde laag af. Magnesiumbicarbonaat zet zich om tot onoplosbare magnesiumhydroxide en koolstofdioxide, conform onderstaande reactie-vergelijking.
Mg(HCO3)2 —> Mg(OH)2 + CO2
Door toepassing van eerder genoemde voorbehandelingsmethoden, worden de calcium- en magnesiumconcentraties uitermate laag gehouden.
Echter als gevolg van een zeer hoge indikking, kunnen van de restconcentraties toch de oplosbaarheidgrenzen worden overschreden. Het magnesiumhydroxide kan zich afzetten als slib.
3.3.3 Calciumfosfaat
Afzettingen van calciumfosfaat ontstaan alleen indien aan calciumhoudend ketelvoedings-water fosfaat wordt toegevoegd. Er vormt zich dan uit mono-, di- of trinatriumfosfaat en calciumzouten het zeer slecht oplosbare calciumhydroxi-apatiet.
Het hydroxi-apatiet zet zich als slib en niet als een harde laag af en wordt grotendeels via de spui uit de ketel verwijderd.
3.3.4 Magnetiet en hematiet
Indien in het ketelwater geen zuurstof aanwezig is, maar wel voldoende alkaliteit, reageert ijzer bij temperaturen boven 120 °C met water, onder de vorming van magnetiet (Fe3O4).
Dit zwarte ijzeroxide vormt een beschermende huid op het metaaloppervlak.
Reactievergelijking vorming magnetiet:
3Fe2+ + 6OH- —> 3Fe(OH)2
3Fe(OH)2 —> Fe2O3.FeO.xH2O + H2 + 2H2O (voorwaarde T > 120 °C)
Fe2O3.FeO.xH2O —> Fe3O4 + xH2O
Als in een later stadium regelmatig zuurstof wordt aangevoerd, wordt het magnetiet afge-broken en omgezet in het niet beschermende hematiet (Fe2O3).
Reactievergelijking vorming hematiet (roest):
4Fe3O4 + xH2O + O2 —> 6Fe2O3. xH2O
3.3.5 Organische vervuilingen
In de ketel gekomen organische vervuilingen vanuit het voedingswater en/of retourcondensaat zullen afhankelijk van de aard van de verbinding en de keteldruk in meer of mindere mate ontleden, waarbij zich dan onoplosbare verbindingen vormen.
Door een vergaande ontleding kan uiteindelijk koolstof ontstaan dat, in verband met zijn sterk isolerend karakter, als afzetting zeer zeker niet gewenst is. Een eenmaal gevormde inerte koolstoflaag is zelfs door middel van een chemische reiniging praktisch niet te verwijderen.
3.3.6 Silicaten
Afzettingen van silicaten kunnen voorkomen in diverse vormen. De eigenschap die dit soort afzettingen gemeen hebben, is dat zij sterk isolerende van karakter zijn en uitermate hardnekkig.
3.4 Opkokers en schuimvorming
Ten gevolge van een te hoge indikking kan het ketelwater gaan schuimen met de volgende problemen:
- De productie van natte stoom ten gevolge van het meegaan van ketelwater met de stoom; dit kan vervuiling van de stoom- en condensaatleidingen betekenen.
- Schuim in contact met het verwarmde oppervlak van de ketel geleidt de warmte niet zo effectief als water, waardoor oververhitting kan optreden.
Detergenten, olie en vetten kunnen eveneens sterke schuimvorming veroorzaken.
Schuimvorming en opkokers kunnen echter ook mechanische oorzaken hebben, zoals:
- Het produceren van stoom bij een lagere druk dan de druk waarvoor de ketels ontworpen.
- Een plotselinge en sterke verhoging van de stoomvraag.
Het aanhouden van een te hoog waterpeil in de ketel geeft opkokers. Schuimvorming kan gesignaleerd worden door een onrustig gedrag van het ketelwater in de peilglazen.
3.5 Corrosie
Op diverse wijzen kan een ketelwatersysteem zowel water- als stoomzijdig door corrosie worden aangetast. Hierna zullen de meest bekende vormen besproken worden.
3.5.1 Zuurstofcorrosie
Zuurstofcorrosie is van alle vormen de meest bekende. Het meest voorkomende corrosieprobleem in het voedingswatersysteem is zuurstofcorrosie, veroorzaakt door een slecht werkende ontgasser. Deze kan aanleiding geven tot pitting, zowel in de ontgasser zelf als in de voedingswaterleiding naar de stoomketel. Daarbij treedt van de diverse deelreacties (zie vorming hematiet) de volgende reactie op, waarbij de putten worden bedekt met roodbruine pokken ijzerroest, het zogenaamde hematiet (Fe2O3).
2 Fe + H2O + O2 —> Fe2O3 + H2
Slecht ontgast ketelvoedingswater zal uiteindelijk ook corrosie veroorzaken in de ketel en het condensaatnet. Het condensaatnet kan op zeer korte termijn worden aangetast, waarbij de corrosie ook kan leiden tot verontreiniging van het ketelwater met ijzeroxidenslib.
Zuurstofcorrosie kan ook optreden tijdens bedrijfsstilstand. Indien het systeem slecht geconserveerd is en een vacuüm in het condensaatnet ontstaat waardoor lucht wordt aangezogen.
3.5.2 Koolstofdioxidecorrosie
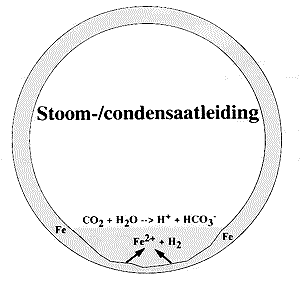
Ten gevolge van de door bicarbonaat- en soda-splitsing ontstane H+ ionen daalt de pH van het condensaat fors. Hierdoor kan aantasting van het staal optreden volgens:
2 H+ + 2HCO3- + Fe —> Fe(HCO3)2 + H2
CO2 corrosie leidt tot een egale aantasting van het staal, in de vorm van een geul.
3.5.3 Loogcorrosie
Een andere vorm van corrosie is de aantasting van koolstofstaal ten gevolge van een te hoge pH, de zogenaamde loogcorrosie. In stoomketels is loogcorrosie een gevolg van een extreem hoge indikking. Daarbij wordt in eerste instantie de beschermende magnetiethuid opgelost, waarna vervolgens loog en water rechtstreeks reageren met het staal onder de vorming van hematiet (roest).
3.5.4 Zuurcorrosie
Ook ten gevolge van een lage pH kan ernstige corrosie ontstaan, namelijk:
- Zuurcorrosie als gevolg van een niet goed uitgevoerde chemische reiniging of nabehandeling.
- Zuurcorrosie als gevolg van het meevoeren van regeneratiezuur met het suppletiewater of inlek van zure producten via het condensaat.
De dosering van de diverse typen conditioneringsmiddelen vindt over het algemeen automatisch en gestuurd plaats, waarbij de dosering bij voorkeur geschiedt in de ketelvoedingwaterleiding aan de zuigzijde van de voedingspomp. Dosering vóór of in de ontgasser wordt in de praktijk ook wel toegepast, waarbij echter dient te worden opgemerkt dat op deze wijze het verbruik van een chemische zuurstofbinder hoger is.
Bepaalde typen conditioneringmiddel dienen rechtstreeks in de stoomleiding geïnjecteerd te worden. In verband met specifieke toepassingen is het derhalve raadzaam het doseerpunt met de waterbehandelaar te bespreken.
Op kleine ketelwatersystemen wordt nog wel eens handmatig gedoseerd, waarbij het nadeel is dat de actieve concentratie dan niet van een constant niveau is en diverse menselijke factoren voor een sterk schommelende dosering kunnen zorgen.
Handmatige dosering is derhalve ter voorkoming van problemen niet aan te bevelen.
5.1 Continue spui
Bij een continue spui wordt een constante hoeveelheid water per tijdseenheid afgevoerd. Deze wijze van spui kan worden toegepast op systemen met een gemiddeld constante belasting. Hierbij wordt echter niet ingespeeld op eventueel wisselende hoeveelheden retourcondensaat, waarbij de maximaal haalbare indikking sterk kan fluctueren.
5.2 Discontinue spui op basis van tijd
Bij een discontinue spui op basis van tijd wordt op gezette tijden automatisch door middels van bijvoorbeeld een tijdgestuurde bodemspui-afsluiter gespuid. Een dergelijk systeem speelt echter niet in op een wisselende belasting van het systeem en op eventuele wisselende hoeveelheden retourcondensaat.
5.3 Discontinue spui op basis van geleidbaarheid
Bij een spui op basis van geleidbaarheid, wordt continu en automatisch door een elektrode de geleidbaarheid van het ketelwater gemeten. Bij het overschrijden van de ingestelde maximaal toelaatbare geleidbaarheid, wordt automatisch een afsluiter open gestuurd, waarna een hoeveelheid gespuid wordt, tot het moment dat de ingestelde geleidbaarheid weer bereikt wordt. Een dergelijk systeem speelt goed in op wisselende belastingen van het systeem.
Voedingwater
| Ketelwater | Tot 0,5 bar | 0,5 tot 20 bar | |
| Keteltype | Alle typen | Vuurgang vlampijp | Waterpijp |
| Uiterlijke hoedanigheid | Helder, kleur- en reukloos | Helder, geen afwijkende kleur of geur | |
| pH minimaal | 7,0 | 7,0 | 7,0 |
| Totale hardheid maximaal (°D) | 0,1 | 0,1 | 0,1 |
| IJzer maximaal (mg/l) | 0,5 | 0,3 | 0,1 |
| Koper maximaal (mg/l) | 0,1 | 0,1 | 0,05 |
| Zuurstof maximaal (mg/l) | 0,1 | 0,1 | |
| Organische stoffen als chemisch zuurstofverbruik | (25) | (25) | (25) |
| CZV maximaal (mg/l) | |||
| Bij een toevoeging van: een moderne organische zuurstof-binder, zoals: DEHA,Hydrochinon,isoascorbinezuur, methylethylketoxine (mg/l) | 0,5 – 1,0 | 0,5 – 1,0 | 0,5 – 1,0 |
( ) = streefwaarde
Ketelwater
| Keteldruk | Tot 0,5 bar | 0,5 tot 20 bar | |
| Keteltype | Alle typen | Vuurgang vlampijp | waterpijp |
| Uiterlijke hoedanigheid | Praktisch vrij van slib, geen afwijkende geur of reuk, weinig of geen neiging tot schuimen. | ||
| p-getal minimaal (meq/l) | 5 | 5 | 5 |
| p-getal maximaal (meq/l) | 10 | 20 | 15 |
| Kiezelzuur (SiO2) maximaal (mg/l) | 15 x p-getal | 15 x p-getal | 15 x p-getal |
| Totaal opgeloste stof uitgedrukt als: | |||
| o Elektrisch geleidingsvermogen bij 20°C, pH 8,3 maximaal (µS/cm) | 4000 | 7000 | 6000 |
| o Soortgelijk gewicht bij 15°C maximaal (°Bé) | 0,4 | 0,7 | 0,6 |
| Organische stoffen als chemische zuurstofverbuik (CZV) maximaal (mg/l) | (100) | (200) | (150) |
| Bij toevoeging van: o Fosfaat (PO43-) |
30 – 80 | 30 – 80 | |
| o Tannine | 100 – 150 | 100 – 150 | 100 – 150 |
| o Sulfiet (SO32-) | 40 – 100 | 40 – 100 | 40 – 100 |
| o Hydrazine (N2H4) | 0,4 – 1,0 | 0,4 – 1,0 | 0,4 – 1,0 |
( ) = streefwaarde

![Stoomketelsysteem[1]](https://www.bewasol.nl/wp-content/uploads/2015/04/Stoomketelsysteem1.gif)